مهر تایید FDA بر داروی زیرجلدی آلزایمر لکمبی Leqembi
تاریخ انتشار :
شنبه ۸ شهريور ۱۴۰۴ ساعت ۱۰:۳۸
کد مطلب : ۱۹۶۲۱
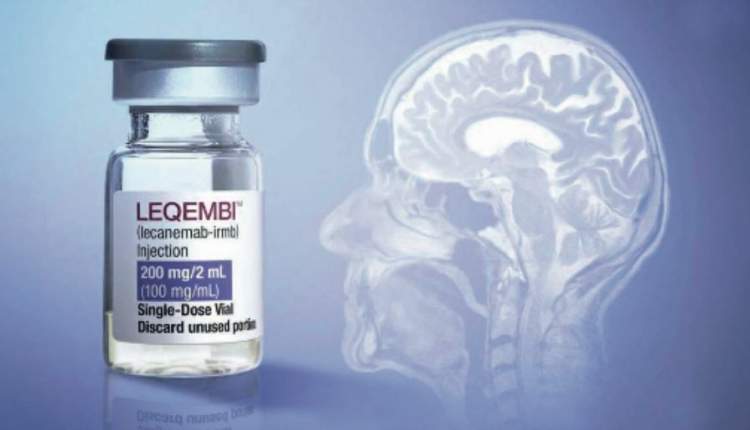
سالمخبر: سازمان غذا و داروی آمریکا FDA شکل تزریقی زیرجلدی داروی Leqembi (lecanemab) محصول مشترک ایزای و بایوژن را برای بیماران مبتلا به آلزایمر تأیید کرد؛ تصمیمی که میتواند جایگاه این دو شرکت را در رقابت شدید با ایلایلیلی برای تسلط بر بازار درمانهای نوین آلزایمر تقویت کند.
Leqembi نخستین داروی ضدآمیلوئید است که سال گذشته مجوز کامل FDA را دریافت کرد و در حال حاضر بهصورت انفوزیون وریدی در دسترس بیماران قرار دارد. شکل جدید زیرجلدی دارو، امکان تزریق آسانتر در خانه یا مراکز درمانی سرپایی را فراهم میسازد و به گفته کارشناسان میتواند میزان پذیرش و دسترسی بیماران را افزایش دهد.
رقابت داغ در بازار آلزایمر
شرکت ایلایلیلی نیز منتظر تصمیم FDA درباره داروی donanemab است که انتظار میرود در ماههای آینده اعلام شود. با این حال، تأیید شکل تزریقی زیرجلدی Leqembi برتری مهمی برای ایزای و بایوژن ایجاد میکند. تحلیلگران بازار پیشبینی میکنند این مزیت میتواند سرعت تجاریسازی و سهم بازار Leqembi را در برابر رقیب اصلیاش افزایش دهد.
دادههای کارآزمایی بالینی نشان دادهاند که Leqembi قادر است با هدف قرار دادن پلاکهای بتاآمیلوئید در مغز، روند پیشرفت آلزایمر را کند کند. شکل زیرجلدی علاوه بر سهولت در استفاده، کاهش بار درمانی برای بیماران و خانوادهها را به همراه خواهد داشت؛ چراکه نیاز به جلسات انفوزیون مکرر و حضور طولانی در مراکز درمانی کاهش مییابد.
کارشناسان معتقدند که رقابت بین ایزای-بایوژن و الیلیلی میتواند به افزایش نوآوری در این حوزه و دسترسی بیماران به درمانهای بهتر منجر شود. تأیید اخیر FDA همچنین گامی مهم در جهت توسعه گزینههای متنوع درمانی برای بیماری آلزایمر است؛ بیماریای که میلیونها بیمار و خانوادههایشان را در سراسر جهان تحت تأثیر قرار داده است.
Leqembi نخستین داروی ضدآمیلوئید است که سال گذشته مجوز کامل FDA را دریافت کرد و در حال حاضر بهصورت انفوزیون وریدی در دسترس بیماران
رقابت داغ در بازار آلزایمر
شرکت ایلایلیلی نیز منتظر تصمیم FDA درباره داروی donanemab است که انتظار میرود در ماههای آینده اعلام شود. با این حال، تأیید شکل تزریقی زیرجلدی Leqembi برتری مهمی برای ایزای و بایوژن ایجاد میکند.
دادههای کارآزمایی بالینی نشان دادهاند که Leqembi قادر است با هدف قرار دادن پلاکهای بتاآمیلوئید در مغز، روند پیشرفت آلزایمر را کند کند. شکل زیرجلدی علاوه بر سهولت در استفاده، کاهش بار درمانی برای بیماران و خانوادهها را به همراه خواهد داشت؛ چراکه نیاز به جلسات
کارشناسان معتقدند که رقابت بین ایزای-بایوژن و الیلیلی میتواند به افزایش نوآوری در این حوزه و دسترسی بیماران به درمانهای بهتر منجر شود. تأیید اخیر FDA همچنین گامی مهم در جهت توسعه گزینههای متنوع درمانی برای بیماری آلزایمر است؛ بیماریای که میلیونها بیمار و خانوادههایشان را در سراسر جهان تحت تأثیر قرار داده است.